Resumen generado por IA
La biología sintética se consolida como un campo revolucionario que fusiona biología, ingeniería, ciencia de datos e inteligencia artificial para diseñar sistemas biológicos con funciones específicas, programando la biología con la lógica del software. A diferencia de la ingeniería genética clásica, que modifica genes puntualmente, la biología sintética diseña sistemas biológicos completos mediante un enfoque modular, predictivo e industrial basado en el ciclo Design–Build–Test–Learn (DBTL). Este proceso iterativo usa modelado computacional, síntesis genética, automatización y aprendizaje automático para crear organismos programables que pueden producir medicamentos, biocombustibles o alimentos de manera eficiente y sostenible.
Las aplicaciones ya son tangibles en salud, energía, agricultura y alimentación. En medicina, impulsa terapias avanzadas, vacunas de ARN y medicina personalizada. En energía, optimiza la producción de biocombustibles y la captura de carbono, mientras que en agricultura mejora cultivos y desarrolla proteínas alternativas con menor impacto ambiental. La inteligencia artificial potencia la biología sintética al acelerar el diseño predictivo y la optimización metabólica, aumentando la eficiencia y reduciendo costos. Sin embargo, este avance requiere una gobernanza sólida para mitigar riesgos bioéticos y ecológicos, garantizando transparencia y acceso equitativo. En conjunto, la biología sintética representa una oportunidad estratégica clave para empresas e inversores, marcando un hito en la bioeconomía y en la transformación industrial hacia la biología programable.
Biología sintética: qué es, cómo funciona y su impacto en salud, energía y alimentación. La ingeniería de la vida que impulsa la bioeconomía.
La biología sintética se consolida como uno de los campos con mayor potencial transformador de la próxima década. Integra biología, ingeniería, ciencia de datos e inteligencia artificial para diseñar sistemas biológicos con funciones específicas. Su ambición es clara: programar la biología con la misma lógica con la que diseñamos software.
En un contexto donde la sostenibilidad, la salud personalizada y la resiliencia industrial marcan la agenda estratégica, la biología sintética emerge como infraestructura tecnológica clave. Este artículo aborda qué es, cómo funciona, en qué se diferencia de la biotecnología clásica y por qué representa una oportunidad estratégica para empresas e inversores.
Definición: ¿qué es la biología sintética?
La biología sintética es una disciplina que aplica principios de ingeniería al diseño y construcción de sistemas biológicos nuevos o rediseñados. Su objetivo es crear organismos, células o circuitos genéticos con funciones específicas y predecibles.
A diferencia de la biología molecular tradicional, que estudia y modifica genes existentes, la biología sintética introduce un enfoque de diseño racional. Se basa en estándares, modularidad y ciclos iterativos de mejora.
Su visión es convertir las células en “fábricas programables” capaces de producir medicamentos, materiales, combustibles o alimentos de forma más eficiente y sostenible.
Biología sintética vs. ingeniería genética clásica
La ingeniería genética clásica se centra en insertar, eliminar o modificar genes en organismos existentes. Su enfoque es correctivo o adaptativo.
La biología sintética adopta una lógica más estructural. Diseña sistemas biológicos completos desde cero o reorganiza los existentes siguiendo principios de arquitectura modular.
Diferencias clave:
- Enfoque: modificación puntual vs. diseño integral.
- Metodología: ensayo-error vs. modelado predictivo.
- Escala: genes individuales vs. redes y circuitos complejos.
- Herramientas: biología molecular tradicional vs. integración con bioinformática e IA.
La edición genética mediante herramientas como CRISPR, desarrolladas y perfeccionadas por centros de referencia como el Broad Institute, ilustra el puente entre ambos mundos. La biología sintética amplía ese enfoque y diseña arquitecturas genéticas completas con funcionalidades emergentes.
El ciclo Design–Build–Test–Learn: industrializar la biología
La biología sintética adopta una lógica industrial. Su motor es el ciclo Design–Build–Test–Learn (DBTL), un proceso iterativo que convierte el laboratorio en una plataforma de innovación continua. Cada vuelta del ciclo genera datos, mejora el diseño y acelera el siguiente experimento.
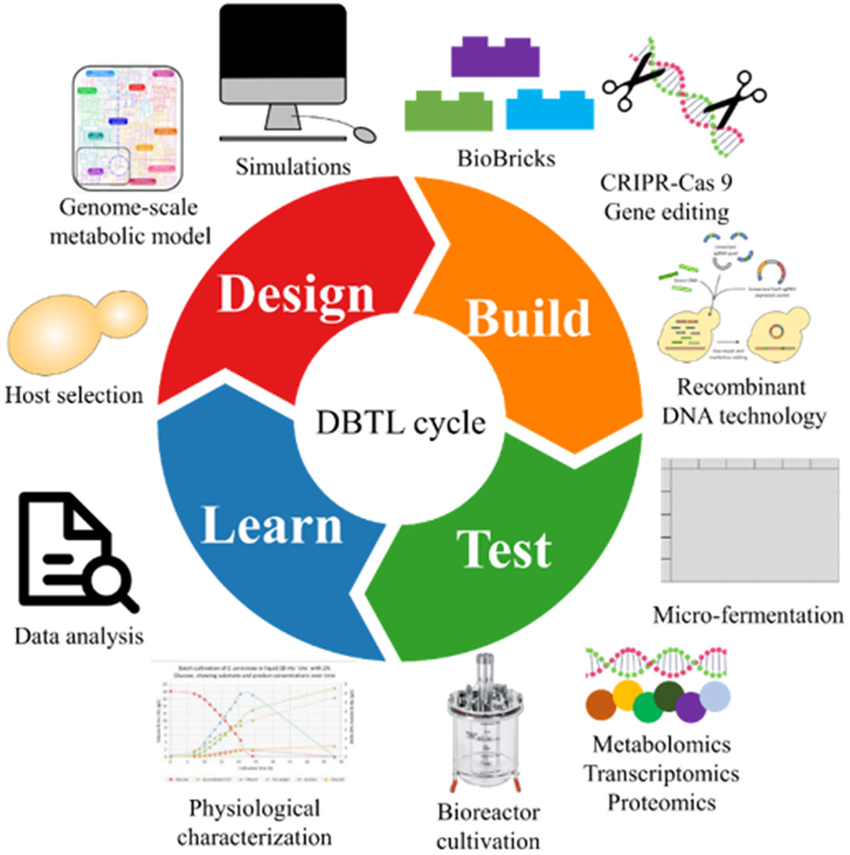
Fuente: ResearchGate
En la fase Design, la biología se modela antes de tocar una pipeta. Equipos multidisciplinares combinan bioinformática, simulación computacional y bases de datos genómicas para diseñar circuitos genéticos con funciones específicas. El diseño se centra en la arquitectura metabólica que permite alcanzar un objetivo concreto: producir una proteína terapéutica, sintetizar un bioplástico o captar carbono con mayor eficiencia.
Aquí la inteligencia artificial juega un papel estructural. Modelos predictivos anticipan cómo se comportará una enzima modificada o cómo interactuarán varios genes en red. El diseño deja de ser artesanal y se aproxima al diseño asistido por ordenador que transformó la industria aeronáutica.
En la fase Build, ese diseño se materializa. La síntesis de ADN ha reducido su coste de forma exponencial en la última década. Empresas especializadas fabrican secuencias genéticas a medida, que luego se ensamblan en microorganismos como bacterias o levaduras. Estas células actúan como chasis biológicos programables. La metáfora es clara: el ADN funciona como código y la célula como hardware vivo.
El salto cualitativo llega en Test. Plataformas automatizadas ejecutan cientos o miles de variantes en paralelo. Sensores, microfluidos y robótica generan datos en tiempo real sobre rendimiento, estabilidad o consumo energético. El laboratorio se convierte en una fábrica de datos.
Un ejemplo ilustrativo es el desarrollo de nuevas rutas metabólicas para producir combustibles sostenibles. En lugar de probar una única combinación genética, los equipos evalúan cientos de configuraciones simultáneamente. Cada experimento alimenta una base de conocimiento creciente.
La fase Learn cierra el ciclo y activa el siguiente. Algoritmos de aprendizaje automático analizan los resultados y detectan patrones que optimizan el diseño posterior. La biología sintética se integra así en un sistema de mejora continua basado en datos. Cada iteración incrementa la eficiencia del sistema biológico diseñado.
Este enfoque ya se aplica en compañías como Ginkgo Bioworks, que ha construido una plataforma industrial para programar microorganismos a escala. Su modelo combina automatización, análisis masivo de datos y diseño iterativo para desarrollar aplicaciones en salud, agricultura o materiales.
El DBTL transforma la biología en una disciplina predecible, escalable y orientada a resultados. Reduce tiempos de desarrollo, optimiza recursos y acerca la biología al lenguaje de la ingeniería.
Principales aplicaciones que ya son realidad
La biología sintética ha dejado el terreno experimental para integrarse en cadenas de valor estratégicas. Salud, energía y alimentación concentran hoy los casos de uso más maduros. En estos ámbitos, la capacidad de diseñar sistemas biológicos con precisión industrial genera impacto tangible en costes, sostenibilidad y velocidad de desarrollo.
Hablamos de aplicaciones que ya operan en el mercado. Plataformas productivas, startups y grandes corporaciones incorporan biología programable como infraestructura tecnológica. La promesa se traduce en resultados medibles.
Salud y medicina
La biología sintética redefine el desarrollo de terapias avanzadas. Las células se convierten en plataformas de producción altamente eficientes. Bacterias y levaduras modificadas sintetizan insulina, hormonas o anticuerpos con estándares industriales. La fabricación biológica gana en precisión y trazabilidad.
Las terapias celulares representan otro salto cualitativo. En los tratamientos CAR-T, las células inmunes del propio paciente se reprograman para identificar y eliminar tumores. Aquí la biología sintética aporta herramientas de diseño de circuitos genéticos que mejoran especificidad y eficacia.
El desarrollo de vacunas basadas en ARN consolida esta tendencia. Moderna demostró durante la pandemia la capacidad de diseñar y escalar una solución terapéutica en tiempos récord gracias a plataformas basadas en biología programable. El modelo se apoya en diseño digital, síntesis rápida y producción flexible.
La medicina personalizada avanza en paralelo. Se diseñan circuitos genéticos que actúan como sensores internos, capaces de activar respuestas terapéuticas en función de biomarcadores concretos. La célula evoluciona hacia dispositivo inteligente.
El impacto combina eficiencia económica y aceleración del time-to-market. La I+D biomédica adopta un enfoque iterativo y data-driven.
Energía y medioambiente
La transición energética requiere soluciones escalables y sostenibles. La biología sintética aporta una vía basada en procesos vivos optimizados.
Microalgas y bacterias modificadas producen biocombustibles avanzados con mayor rendimiento. La captura biológica de carbono mediante microorganismos diseñados abre nuevas oportunidades en la gestión de emisiones industriales. La célula actúa como sumidero activo.
La biorremediación avanza con cepas capaces de degradar plásticos o compuestos contaminantes específicos. En paralelo, la fermentación de precisión impulsa la generación de materiales sostenibles, desde biopolímeros hasta ingredientes industriales de baja huella ambiental.
Compañías como LanzaTech trabajan en la conversión de emisiones industriales en combustibles y productos químicos, integrando biología sintética en procesos de economía circular.
Estas aplicaciones conectan con la agenda climática y con los objetivos de descarbonización industrial. La biología sintética transforma residuos en recursos y redefine la eficiencia de procesos.
Agricultura y alimentación
La seguridad alimentaria se sitúa en el centro de la agenda global. La biología sintética ofrece herramientas para aumentar resiliencia y calidad nutricional.
El arroz dorado ilustra la capacidad de biofortificar cultivos mediante rediseño metabólico. La ingeniería de rutas biosintéticas permite enriquecer alimentos con micronutrientes esenciales. La resistencia a sequías y plagas mejora mediante modificaciones dirigidas que optimizan la respuesta fisiológica de las plantas.
La fermentación de precisión impulsa la producción de proteínas alternativas con menor impacto ambiental. Impossible Foods aplica biología sintética para diseñar proteínas vegetales con propiedades sensoriales similares a la carne tradicional. El objetivo es replicar textura, sabor y valor nutricional mediante diseño molecular. Por otro lado, la carne cultivada, desarrollada a partir de células animales en biorreactores, avanza como categoría emergente en la industria alimentaria.
La convergencia entre biología sintética y foodtech configura un nuevo paradigma agroindustrial. Productividad, sostenibilidad y nutrición se integran en una misma plataforma tecnológica.
El papel de la inteligencia artificial
La biología sintética avanza al ritmo de la inteligencia artificial. La combinación de modelos computacionales, grandes volúmenes de datos biológicos y capacidad de cómputo transforma la forma en que se diseñan sistemas vivos. La disciplina evoluciona desde la experimentación incremental hacia el diseño predictivo.
El diseño de proteínas ilustra este cambio. Comprender cómo una secuencia de aminoácidos adopta una estructura tridimensional concreta ha sido uno de los grandes retos de la biología molecular. Herramientas desarrolladas por DeepMind, como AlphaFold, han demostrado que la predicción estructural puede alcanzarse con una precisión sin precedentes. Este avance impacta directamente en la biología sintética: permite diseñar enzimas y proteínas con funciones específicas antes de sintetizarlas en el laboratorio.
La optimización de rutas metabólicas sigue la misma lógica. Una célula funciona como una red compleja de reacciones químicas interconectadas. La IA analiza millones de combinaciones posibles y propone configuraciones que maximizan la producción de un compuesto concreto o reducen subproductos indeseados. El diseño metabólico deja de basarse en hipótesis aisladas y se apoya en exploración algorítmica a gran escala.
La simulación previa al experimento acelera el proceso. Modelos generativos evalúan millones de variantes de secuencias genéticas antes de construir una sola. Esta capacidad reduce costes, acorta ciclos de desarrollo y aumenta la probabilidad de éxito en fases tempranas.
La IA también identifica patrones invisibles al análisis humano. Detecta correlaciones en datos experimentales masivos, ajusta parámetros en tiempo real y sugiere nuevas hipótesis de diseño. El laboratorio se convierte en un sistema híbrido donde científicos y algoritmos colaboran de forma continua.
En 2026, la biología sintética opera como disciplina plenamente data-driven. La convergencia entre biotech e IA multiplica la velocidad de innovación y redefine la competitividad en salud, energía y alimentación. Quien domine esta integración liderará la próxima ola de la bioeconomía.
Ética y bioseguridad
El potencial transformador exige gobernanza sólida.
Los principales riesgos incluyen:
- Uso indebido con fines de bioterrorismo.
- Impacto ecológico de organismos liberados.
- Concentración de propiedad intelectual.
- Acceso desigual a terapias avanzadas.
Organismos internacionales y comunidades científicas trabajan en marcos de bioseguridad y trazabilidad genética. La transparencia y la cooperación público-privada resultan clave para construir confianza.
La narrativa importa. La aceptación social depende de una comunicación clara y una regulación eficaz.
La bioeconomía: el mercado de la biología sintética
La biología sintética forma parte del núcleo de la bioeconomía emergente. Sectores como pharma, agroindustria, energía y materiales convergen en un mercado que atrae capital riesgo y alianzas estratégicas.
Las previsiones de mercado estiman un crecimiento sostenido durante la próxima década, impulsado por:
- Digitalización del laboratorio.
- Reducción del coste de síntesis de ADN.
- Automatización industrial.
- Demanda de soluciones sostenibles.
Para las empresas, la oportunidad reside en integrar capacidades biológicas en su cadena de valor. Para los inversores, representa una frontera tecnológica comparable al software en los años noventa.
Una disciplina estratégica para el futuro
La biología sintética marca un punto de inflexión en la forma en que interactuamos con la naturaleza. Por primera vez, diseñamos sistemas vivos con una lógica cercana a la ingeniería industrial. ADN como código, células como plataformas productivas y datos como motor de mejora continua. Esta convergencia entre ciencia profunda, tecnología digital y visión empresarial redefine los límites de la innovación.
Su impacto se extiende a sectores estructurales de la economía: salud avanzada, transición energética, seguridad alimentaria y nuevos materiales. Cada uno de estos ámbitos encuentra en la biología sintética una palanca de eficiencia, sostenibilidad y diferenciación competitiva. El resultado es un cambio de escala en la capacidad de crear valor a partir de procesos biológicos.
Para los profesionales de la innovación y la estrategia, comprender esta disciplina implica anticipar una transformación industrial. Las organizaciones que incorporen capacidades de biología programable en su hoja de ruta fortalecerán su posicionamiento en la bioeconomía emergente.
Entramos en la era de la biología programable. El liderazgo se construye desde hoy.



